En ökad förståelse på molekylär nivå av vilka mekanismer som prostatacancerceller använder sig av för att bli rörliga och sprida sig, kan på sikt ge nya möjligheter till behandling av aggressiv prostatacancer.
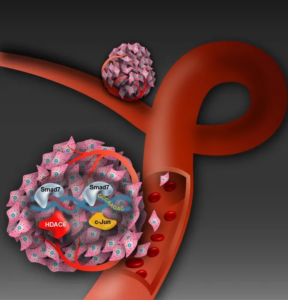
Illustration av hur proteinet Smad7 förstärker utvecklingen av tumörer genom att reglera genuttrycket av HDAC6 och c-Jun. Illustration: Kemal Avican.
Det visas i en ny studie av forskare vid Umeå universitet i samarbete med forskare i Uppsala och Tokyo.
– Vi visar att en specifik aminosyra i en signalmolekyl spelar en viktig roll i att göra cancercellerna mer rörliga och på så sätt bidrar till ökad risk för metastaser, säger Maréne Landström, professor vid Umeå universitet.
Forskningen rör tillväxtfaktorn TGF-β, Transforming Growth Factor Beta, som reglerar hur celler växer och specialiseras. Det är sedan tidigare känt att TGF-β överproduceras i många cancerformer, däribland prostatacancer. Höga nivåer av TGF-β har visat starkt samband med dålig prognos och låg överlevnad. Detta eftersom tillväxtfaktorn stimulerar cancerceller att sprida sig i kroppen och bilda livshotande dottertumörer, metastaser.
TGF-β reglerar uttrycket av proteinet Smad7 som är aktivt i TGF-β-signalkedjan. I friska celler kan Smad7 förhindra fortsatt TGF-β-signalering via negativ återkoppling. Nu kan dock Maréne Landström och hennes forskargrupp och kollegor visa att i cancerceller kan Smad7 tvärtom förstärka utvecklingen av tumörer genom att reglera genuttrycket av HDAC6 och c-Jun.
Den specifika aminosyra som har fångat forskarnas intresse heter Lys102 och finns i Smad7. Denna aminosyra binder till särskilda genreglerande funktioner i DNA för att öka produktionen av genuttrycket HDAC6 och c-Jun.
Det gör att cancercellerna blir mer rörliga och har lättare att bilda dottertumörer, metastaser. Det går att se ett tydligt samband mellan alla dessa komponenter och dålig prognos vid prostatacancer.
– Den goda nyheten är att man genom att behandla med en hämmare av HDAC6 kan få prostatacancercellerna att förlora sin rörlighet. Därmed kan ny möjlighet på sikt öppnas för behandling som minskar risken för metastaser, säger Maréne Landström
Kliniska prövningar genomförs nu i Storbritannien för specifika HDAC6-hämmare för patienter med solida tumörer, vilket gör att behandling med HDAC6-hämmare kan komma att bli ett komplement i cancerbehandling för patienter som har en svårbehandlad sjukdom. Framtida studier kan undersöka nyttan av att påvisa uttryck av Smad7, HDAC6 och c-Junför att möjliggöra nya och mer specifika behandlingar för män med aggressiv prostatacancer.
Studien visar också på en helt ny funktion för Smad7, genom att det kan rekrytera Smad2 och Smad3 till platsen för transkription för dessa gener. Tidigare har man tillskrivit Smad7 rollen av att vara en inhibitor för TGF beta-Smad2/3-transkriptionell aktivitet.



